Innehåll
Andra avsnittVäte är det lättaste elementet och har många industriella användningsområden, inklusive skapande av hydrerade fetter för användning i köket och produktion av kolväten från kol. Det är en väsentlig del av vattenmolekyler och kan separeras med en liten mängd elektricitet. Du kan också producera vätgas med vissa aktiva metaller och starka syror. Båda metoderna är relativt enkla och gör att du kan samla vätgas.
Steg
Metod 1 av 2: Använd vattenförskjutning med aktiva metaller
Samla in nödvändiga material. För att samla väte med reaktionen att blanda en stark syra med en aktiv metall behöver du: en Erlenmeyer-kolv, en gummipropp, plastslang, destillerat vatten, provrör, en stor behållare, 3 molär klorvätesyra (HCl) och magnesium- eller zinkpellets.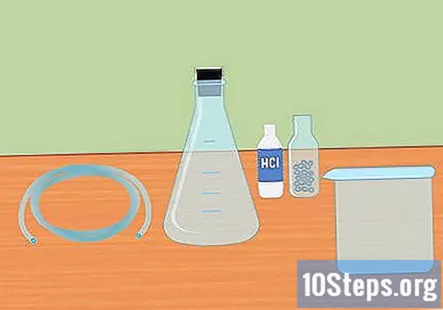
- En Erlenmeyer-kolv är en glaskolv som har en konisk botten och cylindrisk hals.
- Gummiproppen är till toppen av kolven och måste ha ett hål i mitten för att slangen ska gå igenom.
- Antingen magnesium eller zink fungerar för detta experiment, du behöver inte båda.
- En del av dessa leveranser kan behöva köpas online eller i en laboratoriebutik.

Använd lämplig skyddsutrustning. När du arbetar med en stark syra som saltsyra, vill du se till att du vidtar korrekta säkerhetsåtgärder. Det är viktigt att ha på sig en kappa, handskar, slutna tåskor och ögonskydd.- Skyddsglasögon ska vikas runt sidorna på dina ögon för att skydda dem från stänk.
- Använd handskar som passar ordentligt så att du upprätthåller god fingerfärdighet i händer och fingrar.
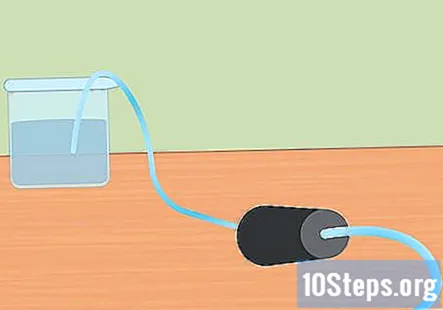
Förbered den experimentella installationen. För in ena änden av slangen i hålet på gummiproppen. Du vill att slangen ska gå hela vägen genom gummiproppen och sticker ut något från slutet. Fyll den stora behållaren med vatten och placera slangens fria ände i vattnet. När experimentet börjar sätter du gummiproppen i Erlenmeyer-kolven.- Lägg dessa bitar åt sidan tills du är redo att använda dem.
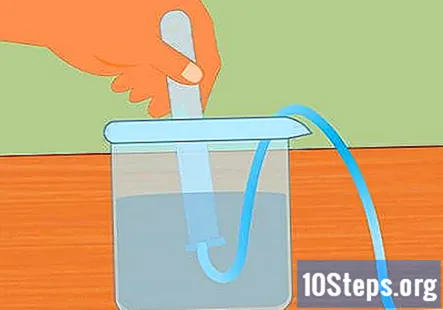
Sänk provröret i vattnet. Ta minst ett provrör (du kan använda mer om du vill samla mer väte) och sänk ner det i vattnet. Luta röret så att alla luftbubblor kan fly. Placera röret ovanpå det nedsänkta slangen som är fäst vid gummiproppen i motsatt ände.- Det är viktigt att alla luftbubblor tas bort från röret innan du börjar. Om de inte är det kommer gasen som samlas in i röret att vara mer än bara väte.
Tillsätt saltsyra till Erlenmeyer-kolven. Tillsätt tillräckligt med saltsyra för att fylla kolven ungefär halvvägs. Cirka 100 ml bör räcka. Se till att kolven är ren och torr innan du tillsätter syran. Använd gummihandskar och var försiktig när du fyller kolven.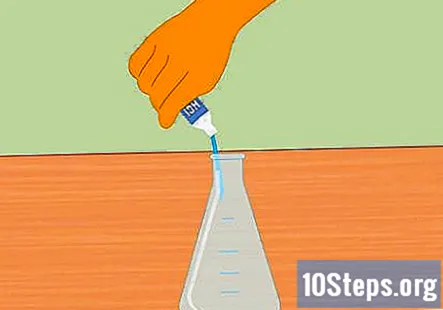
- Var noga med att inte spilla vatten i syran. Vatten tillsatt till syra kan leda till en explosion och skada.
Starta den kemiska reaktionen genom att tillsätta metallpellets till HCl. Tillsätt en handfull zink- eller magnesiumpellets till saltsyran i kolven. Det exakta beloppet du lägger in är inte viktigt, men en liten handfull bör vara tillräckligt för att starta reaktionen.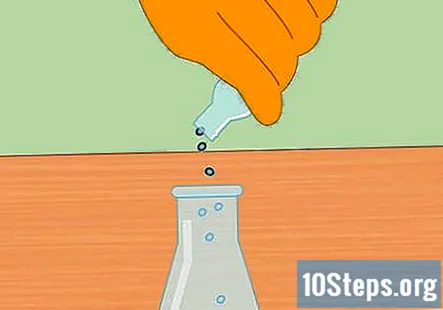
- När du har tillsatt pellets, placera proppen i kolven så att systemet nu är stängt.
Samla väte i ett nedsänkt provrör. När metallen reagerar med syran produceras vätgas. Detta väte färdas till toppen av kolven, genom slangen och in i provröret nedsänkt i vattnet. Gasen kommer att förskjuta vattnet och du bör se en bubbla bildas högst upp på provröret.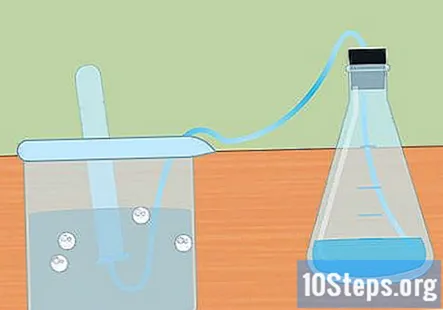
- När provröret fylls med väte, sänk ett annat rör med vatten och placera det över slangen. Du kan samla så mycket väte som produceras av din reaktion.
- Håll provrören nedåt för att förhindra att vätgas släpper ut i luften.
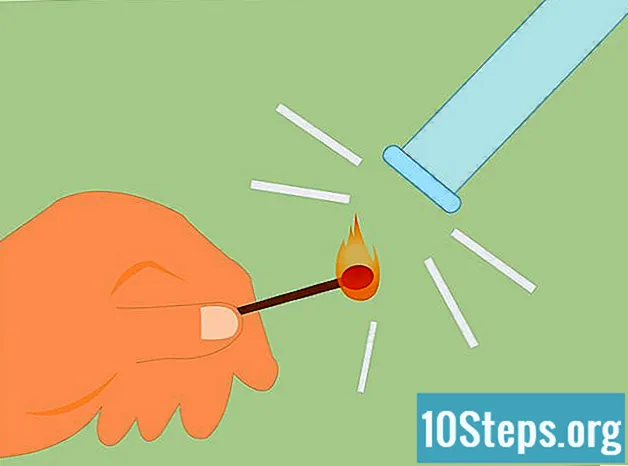
Bekräfta att gasen är väte. För att bekräfta att gasen är väte kan du göra det som kallas splintprovet. Tänd en tändsticka och håll den under röret. Du kommer att höra ett "pop" eller ett pipande ljud som indikerar att det finns väte.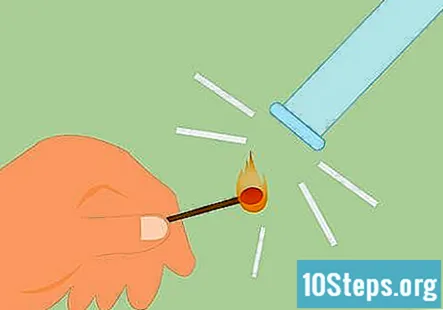
Metod 2 av 2: Använd elektrolys
Samla in nödvändiga material. I detta experiment kommer du att använda elektricitet för att separera väte- och syrgas från vattenmolekyler. För att samla vätgas med elektrolys behöver du ett 9-volts batteri, en penna, två provrör, en plastbehållare, vatten, bakpulver, två stora gummiband (valfritt) och en batteriklämma med klämmor i slutet.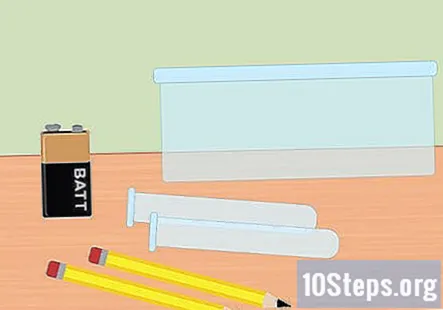
- Pennan måste ha grafit för att det ska fungera. En penna nummer 2 är perfekt. Två små bitar grafit kommer också att fungera för detta.
- En liten behållare eller skål för livsmedel räcker.
- Se till att batteriklämman kan passa ett 9-volts batteri och att den har en röd och svart tråd med krokodilklämmor i slutet. Dessa klämmor används för att ansluta ditt system till batteriet.
Ta bort radergummit från pennan och bryt pennan på mitten. Du behöver två bitar grafit, en för den positiva änden av batteriet och för den negativa änden av batteriet. Vassa båda ändarna av varje bit av pennan till en punkt. Se till att grafiten är väl exponerad.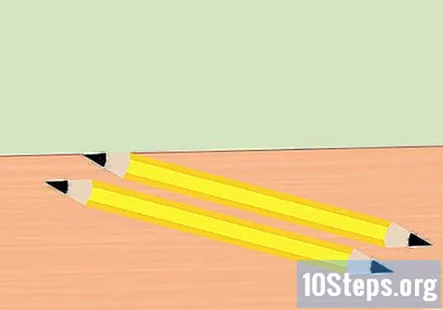
- Detta steg kan hoppas över om du redan har två delar ren grafit.
Vik 2 gummiband runt behållaren i X-form. Detta steg är valfritt, men är ett enkelt sätt att hålla provrören på plats medan experimentet pågår. Sträck ett gummiband över behållaren och sträck ett andra gummiband över det så att det passerar över det första och bildar ett X.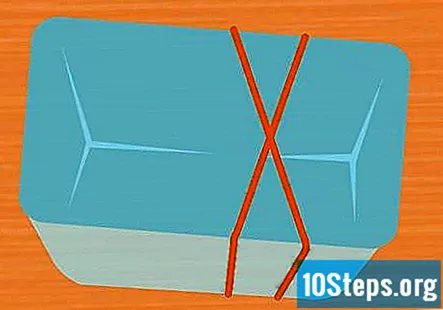
- Om du inte använder gummiband, se till att säkra provrören med tejp eller snöre så att de håller sig upp och ner under experimentet.
Gör en bakpulver och vattenlösning. Att lösa bakpulver i vatten hjälper till att leda elen i systemet. Den exakta mängden tillsatt bakpulver är inte viktig, men cirka 1 tesked per 1 kopp vatten bör vara tillräcklig. Rör om tills det är helt upplöst.
- Använd varmt vatten för att påskynda upplösningen av bakpulver.
Fyll plastbehållaren och provrören med natronlösning. Behållaren måste vara tillräckligt stor för att rymma båda provrören. Tillsätt tillräckligt med lösningen för att fylla behållaren ungefär tre fjärdedelar full. Sänk provrören i lösningen av behållaren och vänd dem upp och ner. Placera varje rör i gummibandets kors X för att hålla det på plats.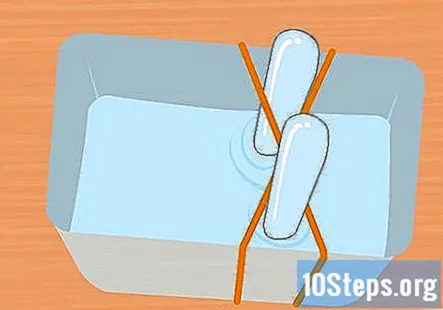
- Det är mycket viktigt att båda provrören är helt fulla av vatten och inga luftbubblor finns kvar.
Fäst krokodilklämmorna på grafiten. Ta en klämma från batteriklämman och fäst den på slutet av en av pennorna. Se till att den rör så mycket av grafiten som möjligt. Gör detsamma med återstående krokodilklämma och penna.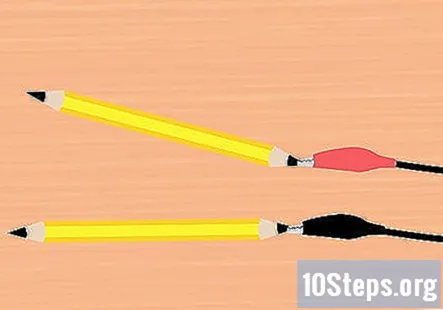
- En penna ska fästas på den röda klämman och en penna på den svarta klämman.
Skjut in den oklämda änden av pennan i provröret. Håll provröret helt nedsänkt och luta det något så att du kan skjuta in den oklämda änden av pennan i röret. Upprepa denna process med den andra pennan och det andra provröret.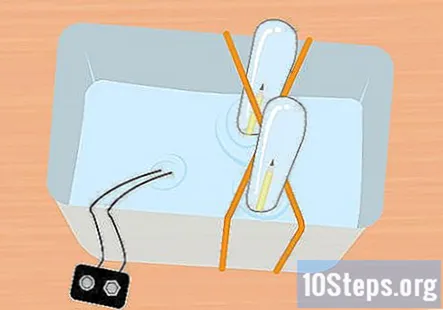
- Vid denna tidpunkt bör allt vara under vattnet och det ska finnas en penna i varje provrör.
- Håll slutet på batteriklämman som fäster på batteriet ur vattnet.
Fäst batteriklämman till 9-voltsbatteriet. Med allt inställt är du nu redo att använda elen från 9-voltsbatteriet. Slutet på batteriklämman ska sticka ut ur behållaren så kläm helt enkelt batteriet på plats. När batteriet är anslutet bör du märka att bubblor stiger från slutet av grafiten och flyter till toppen av varje provrör.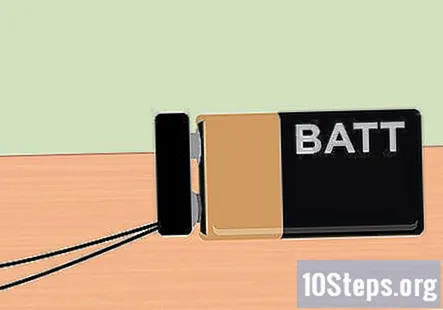
- Om du inte ser bubblor producerade, kontrollera att krokodilklämmorna sitter ordentligt fast vid penns grafit. Kontrollera också att batteriet är fulladdat.
- Provröret med den negativa ledningen fäst vid pennan kommer att producera väte, medan provröret fäst vid batteriets positiva ledning kommer att producera syre.
Samla väte och syre i de två provrören tills du har några centimeter gas i varje rör. Kom ihåg att röret som är anslutet till den negativa änden av batteriet kommer att ha väte och syret kommer att vara i röret anslutet till den positiva änden. Ta bort provrören från burken, en i taget. Håll dem upp och ner och låt vattnet rinna ut. Gasen i rören kommer att förbli trots att du inte kan se den.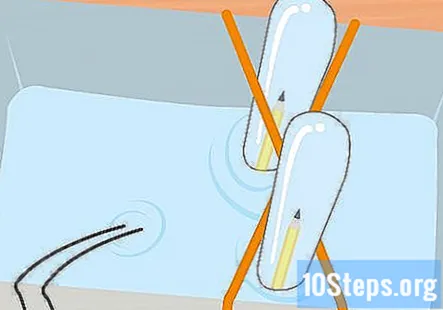
Test för förekomst av väte. Du kan testa om det finns väte genom att slå en tändsticka och hålla lågan upp mot gasen. Det kommer att ge ett väldigt distinkt “knarrigt pop” -ljud om det är väte. Du kan också använda ett tänt ljus istället för en tändsticka.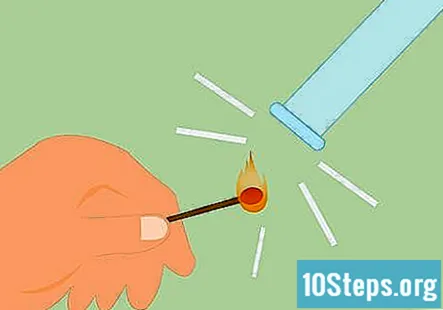
- För att testa syre i provröret som var anslutet till den positiva sidan av strömkällan, blåsa ut en tänd tändsticka (eller ljus) och placera den fortfarande glödande änden under provröret. Om ljuset tänds igen är syre närvarande.
Frågor och svar från gemenskapen
Behöver jag två provrör om jag bara vill samla väte?

Miljöforskare Bess Ruff är doktorand i geografi vid Florida State University. Hon tog sin magisterexamen i miljövetenskap och management från University of California, Santa Barbara 2016. Hon har genomfört undersökningsarbete för marin planeringsprojekt i Karibien och gett forskningsstöd som doktorand för Sustainable Fisheries Group.

Hur mycket väte kan samlas upp från detta enkla elektrolysförsök? Och vad skulle vätgasens tryck vara?
Det beror på. Reaktionshastigheten (vattendelning) baseras på batteriets förstärkare och tiden som återstår att reagera. Vätet skulle vanligtvis ha ungefär havsnivåtryck om du inte gör experimentet i en riktigt varm eller kall miljö.
Varför samlas väte i det negativa röret
På grund av hur vattenmolekylerna delar elektroner är väteatomerna positivt laddade och syreatomerna negativt laddade. När gaserna dras ut kommer det positivt laddade vätet att attraheras av det negativa röret, medan det negativt laddade syret kommer att attraheras av det positiva röret.
Varför flydde inte gasen från mitt gasuppsamlingsrör?
Det är väte, en gas som är lättare än alla andra, inklusive helium, vilket betyder att den kommer att stanna kvar i provröret så länge som den slutna änden av röret är överst eftersom de andra gaserna förskjuter det. Anledningen till att vi använder helium istället för väte är att det inte är brandfarligt. Detta beror på att det är en ädelgas (den har ett fullt valensskal på 8 elektroner) och är därför icke-reaktiv.
Skulle gasen vara mycket brandfarlig?
Ja. Se Hindenburg-katastrofen på YouTube. Zeppelinerna använde väte på grund av att det var den lättaste gasen och ganska lätt att få. Det är också anledningen till att vissa biltillverkare arbetar med vätgasdrivna bilar.
är detta den flytande formen av väte?
Nej - väte i detta experiment kommer att vara gasformigt
Hur gör jag flytande väte? Svar
Varningar
- Var försiktig med rent väte. Det är mycket explosivt när det blandas med luft.
- Se till att all annan luft har tagits bort från utrustningen där du samlar väte.